Klinické studie
Klinické studie - Aktuální
Léčba traumatického a degenerativního postižení kloubní chrupavky prodělala za poslední dekády významný posun, jak na poli vědeckém, tak operačním. Stále však zůstává řada otazníků, které jsou předmětem vědeckého výzkumu a neustálých odborných debat. Výsledkem standardních operačních technik je často pouhé vyplnění defektu vazivovou chrupavkou nebo kloubní chrupavce podobnou tkání, jejíž vlastnosti jsou výrazně horší než u zdravé kloubní chrupavky a která v dlouhodobém horizontu nedokáže obnovit normální funkci kloubu.
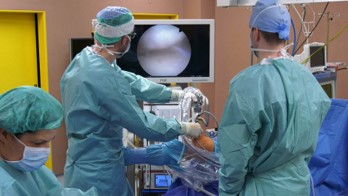
Bioinova se zabývá výzkumem léčby kolenní chrupavky za pomoci kmenových buněk. Tyto buňky mají schopnost dělit se a nahrazovat poškozené a chybějící buňky, čímž přispívají k regeneraci tkání. V chrupavce se kmenové buňky nevyskytují, ale do místa poškození se mohou dostat z kostní dřeně, například při technice mikrofraktur, která se běžně provádí v rámci operačního ošetření defektu chrupavky. Kostní dřeň však obsahuje jen velmi malé množství kmenových buněk (přibližně 0,1 %) a ty jsou někdy dodávány jinými postupy.
Léčba traumatického a degenerativního postižení kloubní chrupavky prodělala za poslední dekády významný posun, jak na poli vědeckém, tak operačním. Stále však zůstává řada otazníků, které jsou předmětem vědeckého výzkumu a neustálých odborných debat. Výsledkem standardních operačních technik je často pouhé vyplnění defektu vazivovou chrupavkou nebo kloubní chrupavce podobnou tkání, jejíž vlastnosti jsou výrazně horší než u zdravé kloubní chrupavky a která v dlouhodobém horizontu nedokáže obnovit normální funkci kloubu.
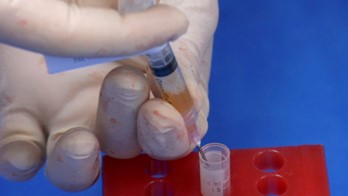
Bioinova se zabývá výzkumem léčby kolenní chrupavky za pomoci kmenových buněk. Tyto buňky mají schopnost dělit se a nahrazovat poškozené a chybějící buňky, čímž přispívají k regeneraci tkání. V chrupavce se kmenové buňky nevyskytují, ale do místa poškození se mohou dostat z kostní dřeně, například při technice mikrofraktur, která se běžně provádí v rámci operačního ošetření defektu chrupavky. Kostní dřeň však obsahuje jen velmi malé množství kmenových buněk (přibližně 0,1 %) a ty jsou někdy dodávány jinými postupy.
Uvedený postup je v současnosti předmětem dvou klinických studií. Tyto studie probíhají dle platné legislativy na základě povolení SÚKL a příslušných etických komisí.
Fáze I (bezpečnost) – VYHODNOCOVÁNÍ
Název: Kmenové buňky z kostní dřeně na 3D nosiči v léčbě poškození kolenní chrupavky. Otevřená klinická studie k určení bezpečnosti a proveditelnosti
Studijní centrum:
Ortopedická klinika a Oddělení sportovní medicíny, Masarykova nemocnice, Ústí nad Labem
Počet pacientů: 6
Délka sledování: 2 roky (celkem 9 vizit)
Současný stav: Probíhá sledování pacientů po aplikaci léčivého přípravku a vyhodnocování výsledků.
Schéma studie:

Fáze II (účinnost) – NÁBOR PACIENTŮ
Název: Účinnost kmenových buněk z kostní dřeně na 3D nosiči v léčbě poškození kolenní chrupavky. Randomizovaná, kontrolovaná, otevřená, multicentrická klinická studie
Studijní centra:
Ortopedická klinika a Oddělení sportovní medicíny, Masarykova nemocnice, Ústí nad Labem
Ortopedická klinika, Fakultní nemocnice Hradec Králové
Klinika ortopedie a traumatologie pohybového ústrojí, Fakultní nemocnice Plzeň
Počet pacientů: 40 (pacienti do 55 let s poškozením kolenní chrupavky a v dobrém celkovém zdravotním stavu)
Délka sledování: 2 roky (celkem 7–8 vizit)
Současný stav: Probíhá nábor pacientů.
Schéma studie:

Klinické studie - Ukončené
Název: Využití autologních multipotentních mesenchymálních kmenových buněk k léčení rozsáhlých defektů skeletu při reimplantaci totální endoprotézy kyčelního kloubu: prospektivní, nerandomizovaná studie k hodnocení bezpečnosti a účinnosti.
Pracoviště: Ortopedická klinika LF UK a FN v Hradci Králové
Hlavní zkoušející: Doc. MUDr. Pavel Šponer, Ph.D.
Zadavatel: Lékařská fakulta Univerzity Karlovy v Hradci Králové
Anotace: Reimplantace totální endoprotézy kyčelního kloubu patří k velmi častým operačním výkonům v ortopedii. Použití autologních či alogenních kostních štěpů při rekonstrukci a léčení kostních defektů během této operace je základním předpokladem pro stabilitu implantátu a dlouhodobé fungování implantované endoprotézy. Problémem aplikace autoštěpů jsou komplikace související s místem jejich odběru, prodloužením operačního výkonu a jejich nedostatečné množství zejména při řešení rozsáhlých kostních defektů. Transplantace alogenních kostních štěpů je provázena rizikem přenosu infekčních onemocnění a odhojení. Konzervací alogenních kostních štěpů se toto riziko snižuje, dochází však k nepříznivému ovlivnění jejich mechanických a biologických vlastností. Moderní metodou, která umožňuje vyloučit nevýhody transplantace autologních a alogenních kostních štěpů, je použití osteokondukčního biomateriálu na bázi trikalcium fosfátu, který slouží jako nosič buněk kostní dřeně. Cílem této studie je hodnocení bezpečnosti a účinnosti kostní novotvorby s využitím beta-trikalcium fosfátového biomateriálu obsahujícího autologní mezenchymální kmenové buňky.
Cíle:
Primární cíl:
Bezpečnost: Hodnocení absence komplikací v místě ošetřeného kostního defektu stehenní kosti, hodnocení případných celkových komplikací.
Sekundární cíl:
Bezpečnost: Výskyt další nutné léčby - rozvoj nepříznivých událostí. Celková bezpečnost.
Účinnost: Hodnocení kvality hojení kostních defektů stehenní kosti pomocí Harrisova kyčelního skóre, rentgenových snímků a denzitometrie, srovnání s referenčními daty.





